Leptospirosis porcina: transmisión y patogenia
Leptospira, como bacteria, no dispone de una membrana impermeable, por lo que su supervivencia depende en gran medida de la humedad del ambiente. En condiciones con una alta actividad de agua, caso de los parques para cerdas gestantes, Leptospira conserva su capacidad infectiva. Las principales vías de entrada de la bacteria en el organismo animal son las mucosas digestiva, respiratoria o genital, así como la conjuntiva ocular y las lesiones que afectan a la integridad de la piel.
vías de entrada de las leptospiras.
Una vez el animal ha sido infectado, Leptospira pasa a torrente sanguíneo, produciéndose una fase de leptospiremia que suele durar entre 7 y 10 días, periodo durante el cual se desarrollará el cuadro clínico propio de cada serovar.
La infección del cerdo por parte de serovares propios de otras especies animales (serovares no adaptados), desencadena un cuadro clínico agudo caracterizado por estados febriles, anorexia, diarrea, hipoagalaxia en cerdas lactantes, cierta ictericia y hemoglobinuria, y un violento cuadro de fallo reproductivo que cursa con tormentas de abortos, aumento de las repeticiones, aparición de cerdas sucias, mortinatos, momias y mortalidad perinatal.
Por otro lado, el cuadro clínico ocasionado por la infección por los serovares adaptados al cerdo, Pomona y Bratislava, puede presentarse de igual manera pero, por lo general, de forma menos virulenta. Cuanto se trata de la primo-infección de una granja negativa se suele dar un cuadro clínico subagudo muy parecido al propio de los serovares no adaptados al cerdo. En cambio, cuando la infección ocurre en una granja positiva, la sintomatología es mucho menos evidente pudiendo parecer, incluso, un proceso asintomático.
En el caso de infecciones por serovares adaptados, el patrón de fallo reproductivo es más insidioso que abrupto. Se caracteriza por un aumento del valor “litter scatter” o camadas anormalmente cortas. Aunque un aumento de este parámetro conlleve importantes repercusiones económicas, puede pasar desapercibido sobre todo en explotaciones con genéticas poco prolíficas o poco tecnificadas, asumiéndose como una producción sub-óptima. Las líneas rojas que no se deben superar y que nos pueden poner en la pista sobre un proceso de leptospirosis por serovares adaptados se establecen en un 15% de litter scatter en cerdas multíparas y un 18% de las camadas procedentes de primerizas.

A continuación de la fase de leptospiremia, la bacteria coloniza distintos órganos como el hígado, estructuras del sistema nervioso central, útero en hembras y vesículas seminales en machos y riñón. Éste último constituye el auténtico órgano diana de la enfermedad y punto clave en el ciclo biológico de Leptospira ya que, después de su división dentro del organismo del cerdo, Leptospira necesita ser excretada al exterior a través de la orina (leptospiruria) para ocasionar nuevas infecciones. En el caso de los serovares no adaptados la fase de leptospiruria tiene una corta duración, mientras que los serovares adaptados establecen un acantonamiento en el tejido renal que prolonga la fase de leptospiruria prácticamente de por vida.
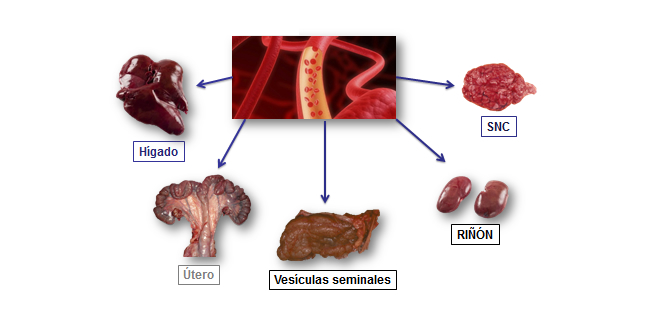
Por su localización Leptospira también puede ser excretada y eliminada al exterior a través del semen, abortos y anejos fetales.
Álvaro Aguarón & Clara Farré. Servicio Técnico de Porcino de Laboratorios Syva, S.A.U
联系
请使用以下表格来联系我们。

